近日,医学影像学院微流控技术与先进材料科研团队在国际顶级学术期刊《Nature Communications》(《自然·通讯》,中国科学院一区Top期刊,IF=15.7)发表了题为《A mechanophenotyping chip for high-throughput detection of metastatic bacteria-infected circulating tumor cells》的研究论文。皖南医学院高彦峰老师为本文的共同第一作者,皖南医学院为该项研究的共同完成单位。
近年来的研究表明,肿瘤组织内定植的细菌与癌症进展密切相关。部分胞内细菌能够通过重组宿主细胞的骨架结构、降低细胞硬度,使癌细胞具备更强的变形能力,从而更易穿过微血管、在循环系统中生存并促进远端转移。然而,如何从海量血细胞中高效捕获并精准识别这些极其稀有且高度可变形的“被感染循环肿瘤细胞”,一直是液体活检和癌症预后评估领域的重大难题。
为解决上述难点,研究团队创新性地研发了一种基于细胞力学表型筛选的微流控芯片(LesM)。该芯片设计有密集的L型微陷阱阵列,其核心原理在于利用被细菌感染的循环肿瘤细胞(CTC)因其细胞骨架重组而变得更“柔软”、更具变形能力的特性。当细胞流经芯片时,所有CTC均可被L型结构捕获,但只有柔软、易变形的感染细胞能够挤过狭窄的变形通道,而刚性较高的细胞则停留在陷阱入口处,形成力学生物标志物的差异化读出。
研究结果表明,LesM芯片的单细胞捕获效率平均高达95.42%,在区分感染与非感染乳腺癌细胞方面特异性达到85.34%。该平台能够一次性对超过10,000个细胞的力学特征和微生物携带情况进行高通量分析,其检测结果与动物模型体内的转移风险及抗生素治疗效果高度吻合。尤为重要的是,研究团队利用LesM芯片在未经处理的全身血样本中成功检测到了被细菌感染的CTC,并通过平行进行的体内转移实验验证了其临床应用的巨大潜力。此外,研究还发现,在原发性肿瘤切除前使用抗生素清除肿瘤内细菌,能显著减少CTC数量并降低肺转移发生率。
该研究开创性地将生物力学与肿瘤内微生物检测相结合,为预测乳腺癌远处转移和指导抗菌疗法提供了一种变革性的液体活检工具。LesM芯片作为一种高通量、省时且高效的策略,不仅极大地推动了癌症基础研究,也为未来的精准医疗和即时诊断开辟了新的方向。(高彦峰/文、图)
原文链接:https://doi.org/10.1038/s41467-025-68152-y
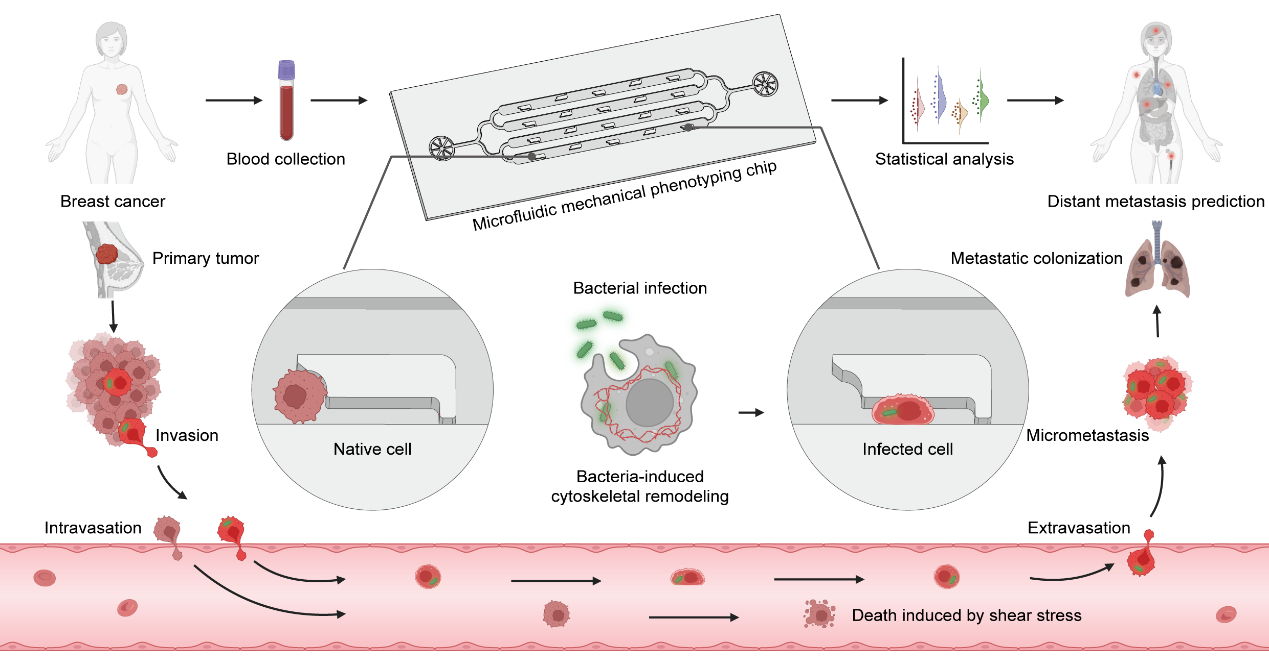
基于细胞力学表型的微流控芯片用于筛选预测乳腺癌转移风险



 皖公网安备 34020302000135号
皖公网安备 34020302000135号