近年来,全球男性生育力下降已成为亟待解决的公共卫生问题。环境重金属污染,特别是镉的广泛暴露,被认为是导致男性生殖功能损伤的关键风险因素之一。尽管环境重金属对男性生殖健康的影响已得到公认,但其从分子干扰、细胞功能障碍到组织病理损伤的完整作用机制,仍缺乏系统性的解析。
近日,我校青年教师李浩联合安徽医科大学公共卫生学院王华教授团队在这一领域取得系列突破性进展,通过三篇分别发表于Science Advances、Environmental Science & Technology及Cell Biology and Toxicology的研究论文,从“关键毒性通路确证—细胞保护机制失效—核心有害结局路径识别”三个维度,层层递进地揭示了镉诱导男性不育的复杂机制网络,为精准干预和靶向防治提供了重要理论依据。
一、确证关键毒性通路:附睾巨噬细胞衰老介导环境应激下的精子活力下降
精子活力是男性生育能力的重要评价指标之一,是精子穿透卵子实现受精的关键动力。依托安徽男性生殖健康队列的人群横断面分析,团队鉴定出铅、镉和汞是导致精子活力下降的关键重金属混合物;通过构建联合暴露小鼠模型,发现铅、镉和汞联合暴露可诱发附睾巨噬细胞衰老并降低精子活力;结合衰老巨噬细胞清除及过继转移实验,证实附睾巨噬细胞衰老是介导精子活力降低的关键事件。机制上,联合暴露抑制去甲基化酶FTO,增加Foxo3 mRNA的m6A修饰,致其表达下调并诱导附睾巨噬细胞衰老;干预FTO或m6A修饰可逆转该过程。这一发现首次揭示了附睾免疫微环境衰老是环境应激导致男性不育的新机制,为弱精症的干预提供了全新策略和理论基础。上述研究成果发表于国际权威期刊Science Advances(Science子刊,综合性一区TOP,IF=12.5),我院青年教师李浩为该论文共同第一作者(排名第二),皖南医学院为第三完成单位。
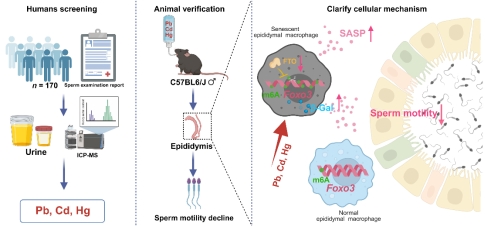
论文相关图片(一)
二、揭示细胞内在守护者:ATG5依赖的自噬是抵抗镉破坏血睾屏障的关键防线
在明确环境混合物效应后,研究进一步聚焦于单一经典毒物——镉,探索其对睾丸核心结构“血睾屏障”的破坏机制。血睾屏障由支持细胞紧密连接构成,是保障精子正常发生的“生命防线”。研究发现,镉暴露会激活支持细胞中的趋化因子CXCL2,进而破坏血睾屏障完整性;而细胞内的“清洁回收系统”——ATG5依赖的自噬,能够通过抑制CXCL2/CXCR2轴,发挥保护作用;当利用基因敲除技术特异性敲除支持细胞中的Atg5基因后,镉对血睾屏障的破坏效应显著加剧。该研究从细胞自我保护的角度,阐明了自噬在抵抗环境毒物中的关键地位,提示增强自噬可能是维护血睾屏障完整性的潜在干预手段。相关成果发表于毒理学领域权威期刊Cell Biology and Toxicology(医学三区[毒理学一区],IF=5.9),我院青年教师李浩为该论文第一作者,皖南医学院为第一完成单位。
原文链接:https://link.springer.com/article/10.1007/s10565-025-10089-5
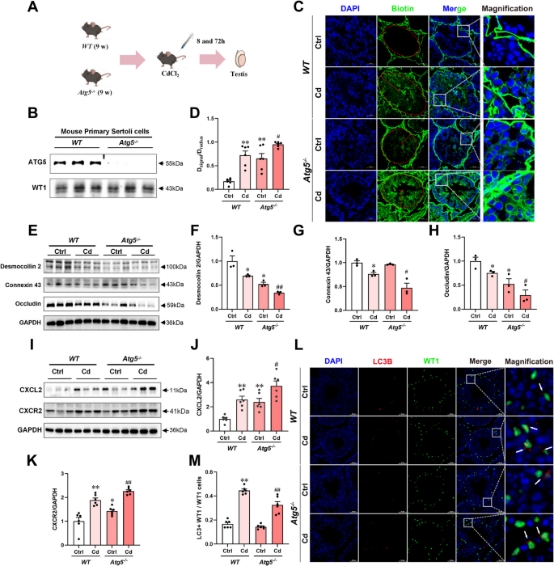
论文相关图片(二)
三、整合多维度证据:锁定PPARα激活介导的睾酮降低作为镉致不育的关键有害结局路径
在积累了众多机制发现(氧化应激、自噬、炎症、表观遗传等)后,研究面临一个更深层的科学问题:在复杂的机制网络中,究竟哪一条是起决定性作用的“主干机制”?为回答这一问题,研究创新性地采用“干湿结合”的多维度整合策略,整合了比较毒理组学数据库(CTD)、AOP-WiKi数据库、NHANES人群调查数据以及体内外实验验证,构建了镉诱导男性不育的有害结局路径(AOP)网络;通过大数据筛选与实验验证发现,尽管存在多条路径,但PPARα激活介导的睾酮合成抑制是整个网络中最关键的核心事件;分子对接和动力学模拟进一步证实,PPARα抑制剂GW6471能够竞争性抑制镉与PPARα的结合。该研究从AOP网络的角度,识别出镉致男性不育的关键分子起始事件与核心有害结局路径,为后续的精准干预提供了高优先级靶点。相关成果发表于环境毒理领域顶级期刊Environmental Science & Technology(环境科学与生态学一区TOP,IF=11.3),我院青年教师李浩为该论文共同第一作者(排名第二),皖南医学院为第二完成单位。
原文链接:https://pubs.acs.org/doi/10.1021/acs.est.5c09190

论文相关图片(三)
系列研究成果不仅系统深化了对环境有害因素暴露致男性不育机制的理解,也为环境相关生殖健康风险的评估与防治提供了多维度的理论支撑和潜在干预策略。上述研究工作得到了国家重点研发计划、国家自然科学基金、安徽省高校自然科学优秀创新团队项目与皖南医学院博士科研启动基金等项目资助。(李浩/文、图)



 皖公网安备 34020302000135号
皖公网安备 34020302000135号