近日,医学影像学院微流控技术与先进材料科研团队在国际材料领域顶级期刊《Advanced Materials》(IF=26.8,新锐期刊分区一区Top期刊)上发表了题为“High-Entropy Alloy Synergized with Gene Editing for Cocktail-Sensitized Radioimmunotherapy of Lung Metastases”的研究论文。医学影像学院医学工程学教研室高彦峰为论文共同通讯作者,皖南医科大学为共同通讯单位。
为应对肿瘤治疗效果受限的问题,放射治疗作为当前临床最重要的抗肿瘤手段之一,主要通过电离辐射直接破坏DNA结构,或间接诱导产生大量活性氧(ROS)以杀伤肿瘤细胞。尽管围绕提升疗效并降低对正常组织损伤的研究已开展了大量探索,肿瘤细胞仍可通过激活DNA损伤修复与细胞周期调控机制产生放疗抵抗,同时高剂量辐射亦会对正常组织造成不可忽视的损伤。因此,如何在降低辐射剂量的前提下显著提升放疗效果,并增强对远端转移灶的抑制能力,已成为肿瘤放疗领域亟待突破的关键科学问题。
目前,针对上述挑战,研究团队创新性地构建了一种集高熵合金放疗增敏、CRISPR/Cas9基因编辑、生物正交免疫激活以及微流控芯片分析技术于一体的多功能纳米治疗平台(HAEPRC)。该平台以由金(Au)、铋(Bi)、铂(Pt)、银(Ag)和钯(Pd)组成的高熵合金为核心,通过肿瘤细胞膜包裹实现同源靶向,并负载靶向PLK1的CRISPR/Cas9系统,实现对肿瘤细胞周期的精准干预与调控。
为实现多层级协同增效,该体系的核心创新体现在多机制的有机耦合:一方面,高熵合金利用多种高原子序元素的“鸡尾酒效应”,显著增强X射线的能量沉积和ROS生成,从物理层面提升放疗增敏效果;另一方面,基因编辑模块通过下调PLK1表达,使肿瘤细胞阻滞于对放疗高度敏感的G2/M期,从而将放疗耐受细胞转化为放疗敏感细胞。同时,平台中的钯元素可通过生物正交催化将前药Pro-I原位转化为免疫激活分子IMD,促进树突状细胞成熟、诱导巨噬细胞向抗肿瘤M1型极化,并增强CD8+ T细胞介导的免疫反应,实现放疗与免疫治疗的协同增强。
按照细胞精细化分析的研究需求,研究团队进一步结合自身在微流控领域的技术积累,设计并构建了“Material Uptake Assay Chip”,用于在单细胞尺度定量评估纳米平台的细胞摄取行为与靶向特异性。通过在芯片微腔中分别培养4T1、B16、RAW 264.7及HUVEC等不同类型细胞,并引入荧光标记的HAEPRC,研究人员实现了对不同细胞类型纳米材料摄取效率的快速、精准比较。实验结果表明,HAEPRC在同源肿瘤细胞中的摄取效率显著高于其他细胞类型,验证了其优异的肿瘤靶向能力。该微流控芯片不仅提高了实验的通量和重复性,也为纳米药物体内行为预测提供了重要工具。
纳米平台的整体性能在后续实验中得到进一步验证。结果显示,在X射线照射条件下,该平台能够显著提高肿瘤细胞内ROS水平和DNA损伤程度,并有效抑制肿瘤细胞增殖。同时,基因编辑效率稳定,PLK1表达显著下调,验证了其在细胞周期调控和放疗增敏中的关键作用。在动物实验中,HAEPRC联合放疗及Pro-I治疗显著抑制肿瘤生长,延长小鼠生存期,并表现出良好的生物安全性。
在原发肿瘤伴肺转移模型中,该联合治疗策略不仅能够有效抑制原发灶生长,还可显著降低肺部转移结节数量,几乎完全消除转移信号。免疫学分析显示,该体系能够显著促进树突状细胞成熟,提高M1/M2巨噬细胞比例,增强CD8+ T细胞浸润,同时降低免疫抑制性Treg细胞水平,表明其能够有效激活系统性抗肿瘤免疫反应,从而实现对远端转移灶的强效抑制。
该研究首次将高熵合金材料引入肿瘤放疗增敏领域,并与基因编辑、生物正交催化及微流控芯片技术有机融合,构建了“物理增敏—分子调控—免疫放大—芯片评价”一体化研究体系。研究成果不仅为提高低剂量放疗疗效和抑制肿瘤转移提供了新思路,也体现了我校在微流控与纳米医学交叉融合领域的持续创新能力。(高彦峰/文、图)
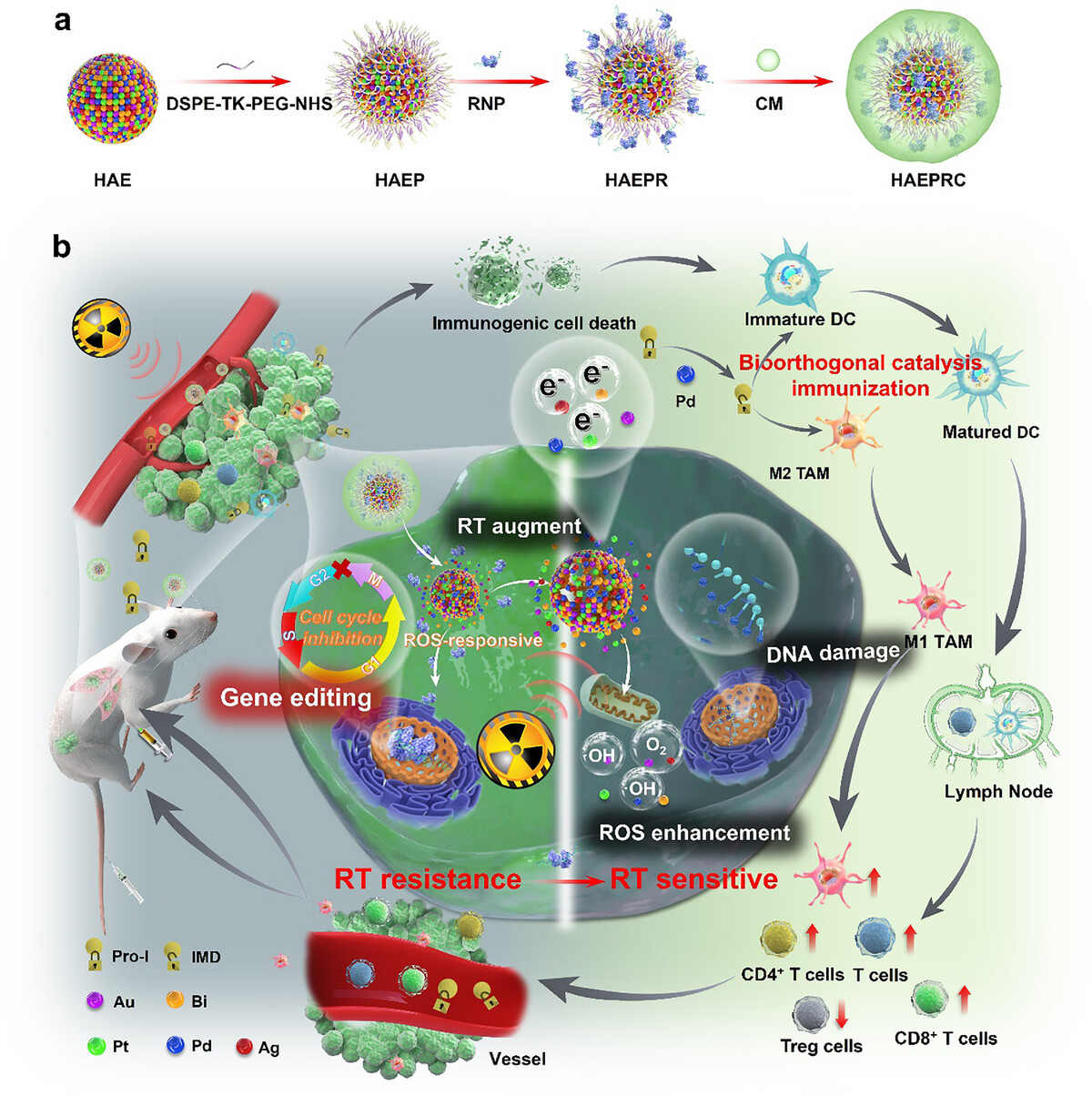
高熵合金协同基因编辑与微流控芯片评价的放射免疫治疗策略示意图
原文链接:https://doi.org/10.1002/adma.202522618



 皖公网安备 34020302000135号
皖公网安备 34020302000135号